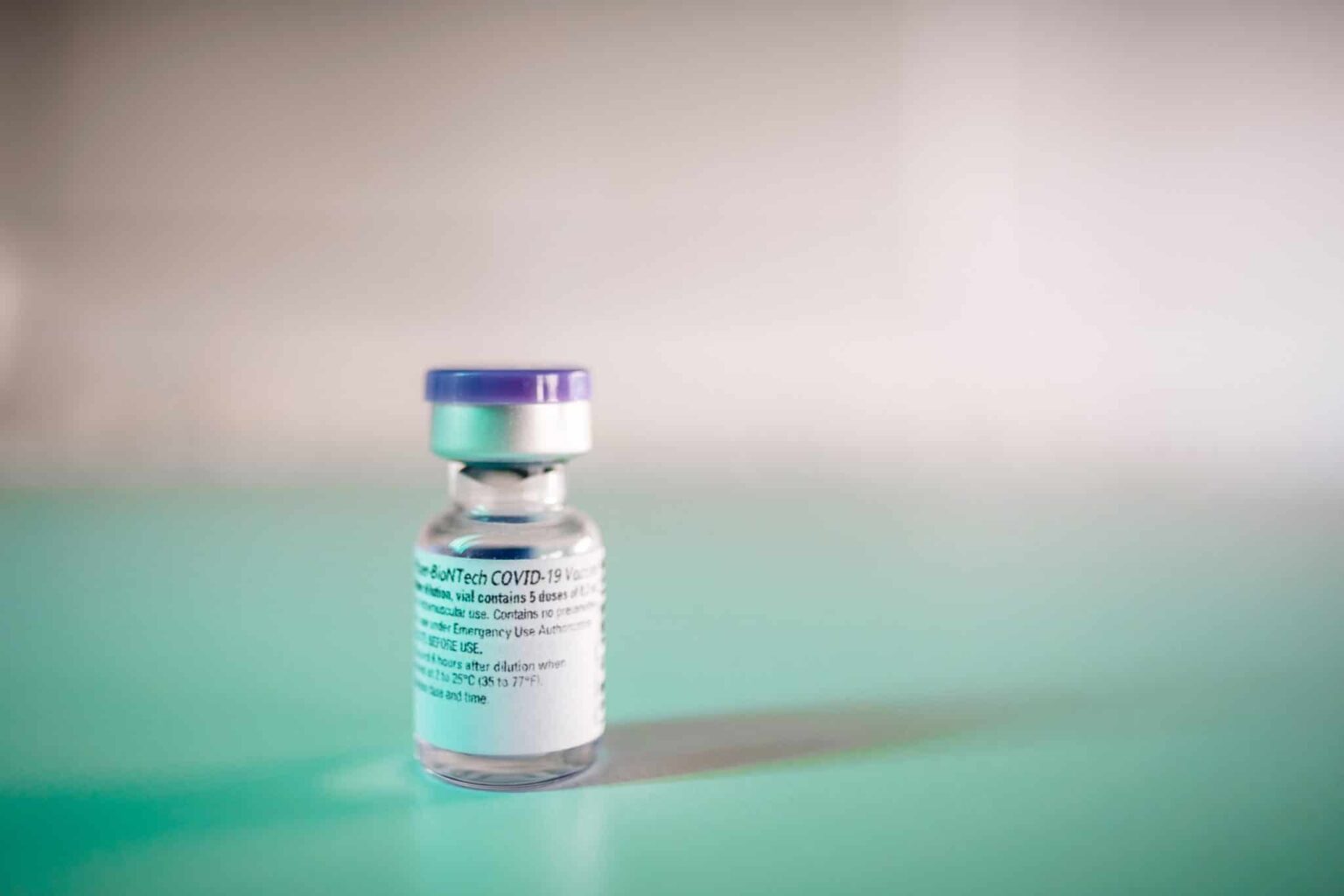
Bereits vor einer Woche wurde in Großbritannien die Erste Patientin, eine 90-jährige Frau, mit dem in Deutschland entwickelten Impfstoff, geimpft.
Mittlerweile wurde das Vakzin auch in den USA, Kanada, Saudi-Arabien, Israel und Bahrein zugelassen. In Europa hingegen lässt die Zulassung weiter auf sich warten.
Wie Bundeskanzlerin Angela Merkel (CDU) am Sonntag mitteilte, soll die Zulassung am 29.12.2020, eventuell ein paar Tage früher, erteilt werden, damit auch in Europa mit der Impfung der Hochrisikogruppen begonnen werden kann.
Die Verzögerung gefällt Bundesgesundheitsminister Jens Spahn nicht, denn er macht mittlerweile Druck auf die Behörde in Brüssel. Noch am 10. November erklärte er, dass er „es als deutscher Gesundheitsminister nur schwer erklären könnte, wenn in anderen Regionen der Welt ein in Deutschland produzierter Impfstoff schneller verimpft würde als in Deutschland selbst“.
Doch genau an diesem Punkt sind wir mittlerweile angekommen. Dies dürfte auch der Grund sein, weswegen er, ebenfalls am Sonntag sagte, dass ein „nationales Zulassungsverfahren schneller“ sei und dass „Bund und Länder ab dem 15.12. in der Fläche einsatzbereit“ seien. „Erste Impfdosen stehen quasi bereit und könnten direkt nach der Zulassung verimpft werden“, so der Bundesminister weiter.
Auch wenn eine nationale Zulassung schneller gehen könnte, verlässt sich die Bundesregierung, aber auch alle anderen europäischen Länder, auf die europäische Behörde. Diese prüft die von BioNTech und Pfizer vorgelegten Daten zum Impfstoff gerade in einer zweiten Schleife.
Dies dauert länger, erhöht jedoch auch die Sicherheit in den Impfstoff, womit auch das Vertrauen der Bürgerinnen und Bürger steigen dürfte.
Ob die „EMA“ nun „nur langsamer“ als die Kollegen in anderen Ländern ist, oder ob es tatsächlich an der genaueren Prüfung der Daten liegt, ist unklar.
Sicher ist auf jeden Fall eins: Es wird bis zur Zulassung des Impfstoffs bereits erste Erfahrungswerte aus den bereits impfenden Ländern geben. Diese können in die Bewertung des Impfstoffs mit einfließen. Dies steigert das Vertrauen in das Vakzin und erhöht die Impfbereitschaft in der Bevölkerung.
Auch muss sichergestellt sein, dass bei der Zulassung von Impfstoffen immer wissenschaftliche Argumente den wirtschaftlichen Aspekten überwiegen. Ob dies in den anderen Ländern der Fall ist, ist unklar und es könnte nur darüber spekuliert werden.
Wichtig ist, dass der Impfstoff bestmöglich geprüft und dann schnellstmöglich geimpft werden kann. Hierfür haben Bundeswehr, Gesundheitsämter und Ehrenamtsinstitutionen den Grundstein gelegt. Alles ist vorbereitet.
Nun braucht es nur noch die Zulassung der Behörde.
Bildquellen
- BioNTech Impfstoff BNT162: BioNTech SE 2020, all rights reserved